|
||
|
立体选择性羰基还原酶及其在手性醇合成中的应用
化工进展
2021, 40 (3):
1142-1160.
DOI:10.16085/j.issn.1000-6613.2020-2124
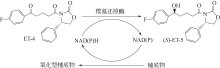
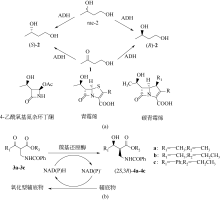
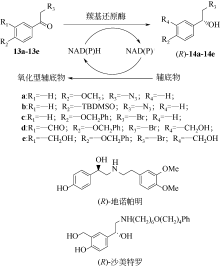
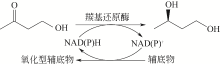
手性醇是重要的医药中间体与精细化工品,立体选择性羰基还原酶催化制备手性醇具有重要的研究与应用价值,受到国内外科学家和工程师的高度关注。本文主要围绕羰基还原酶的发现与分类、催化羰基还原反应的活性与立体选择性机制、酶的筛选挖掘与分子改造技术、辅酶还原型烟酰胺腺嘌呤二核苷酸(磷酸)的再生方法、羰基还原酶催化合成手性醇医药中间体与精细化学品技术开发与应用等方面展开综述。重点阐述了羰基还原酶催化制备降血脂、抗细菌或病毒感染、抗肿瘤、抗抑郁症、抗癫痫等重要疾病治疗药物中间体及脂肪族、芳香族手性醇精细化工品的国内外技术进展与应用,为高效能立体选择性生物催化剂的创制和手性化合物的生物合成提供理论借鉴和成功范例。  View image in article
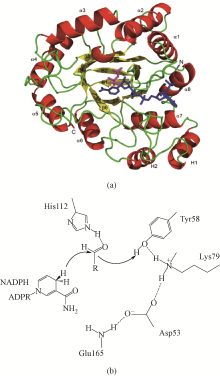
图2
来源于Thermus sp. ATN1的中链脱氢酶TADH三级结构示意图[
正文中引用本图/表的段落
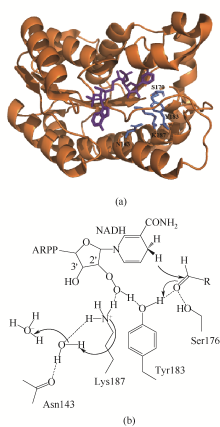
中链脱氢酶(MDRs)是一类约含350个氨基酸残基的锌或非锌-依赖型脱氢酶。根据迭代隐马尔可夫模型(HMMs),中链脱氢酶可分为86类,包括MDR001-ADH、MDR002-PTGR、MDR003-FAS及MDR010-CAD等,不同种类间序列同源性在40%~90%之间。中链脱氢酶一般是以单聚体、二聚体或四聚体的形式存在。每个亚基含有两个结构部分[图2(a)][25],N端与C端共折叠区域形成一个裂缝结构,为活性中心口袋,辅酶结合域覆盖了包括Rossman结构在内的C端大部分区域 [26-28]。细菌中的中链脱氢酶通常为非锌-依赖型,而真核生物中的中链脱氢酶一般为锌-依赖型[29-30]。锌离子有多种结合方式,有的辅酶结合域和活性中心均结合一个锌离子,有的只有活性中心结合一个锌离子,有的则不需要锌离子。中链脱氢酶的催化过程往往需要锌离子的参与,锌离子一般与Cys、His、Asp及一个水分子形成一个含羧基配体的四面体结构,参与酶与底物的结合过程[27]。中链脱氢酶催化醛酮还原的过程中,羰基底物首先进入活性中心,与活性中心His、Ser和His残基连接的Zn+及辅酶核糖环上的两个羟基作用稳定构象,接收来自还原型辅酶C4位上的[H],转化为对应的醇产物[图2(b)][28]。
中链脱氢酶(MDRs)是一类约含350个氨基酸残基的锌或非锌-依赖型脱氢酶.根据迭代隐马尔可夫模型(HMMs),中链脱氢酶可分为86类,包括MDR001-ADH、MDR002-PTGR、MDR003-FAS及MDR010-CAD等,不同种类间序列同源性在40%~90%之间.中链脱氢酶一般是以单聚体、二聚体或四聚体的形式存在.每个亚基含有两个结构部分[ Structural basis for stereo-specific catalysis in NAD+-dependent (R)-2-hydroxyl glutarate dehydrogenase from Acidaminococcus fermentans 1 2005 ... 短链脱氢酶(SDRs)是一种非金属依赖酶,一般含有250~350个氨基酸残基.自19世纪70年代发现昆虫乙醇脱氢酶和细菌核糖醇脱氢酶以来,短链脱氢酶数量不断扩充,目前GenBank数据库中收录的短链脱氢酶的数量已超过99000种[ NAD-binding domains of dehydrogenases 1 1995 ... 短链脱氢酶(SDRs)是一种非金属依赖酶,一般含有250~350个氨基酸残基.自19世纪70年代发现昆虫乙醇脱氢酶和细菌核糖醇脱氢酶以来,短链脱氢酶数量不断扩充,目前GenBank数据库中收录的短链脱氢酶的数量已超过99000种[ Critical residues for structure and catalysis in short-chain dehydrogenases/reductases 2 2002 ... 短链脱氢酶(SDRs)是一种非金属依赖酶,一般含有250~350个氨基酸残基.自19世纪70年代发现昆虫乙醇脱氢酶和细菌核糖醇脱氢酶以来,短链脱氢酶数量不断扩充,目前GenBank数据库中收录的短链脱氢酶的数量已超过99000种[
中链脱氢酶(MDRs)是一类约含350个氨基酸残基的锌或非锌-依赖型脱氢酶.根据迭代隐马尔可夫模型(HMMs),中链脱氢酶可分为86类,包括MDR001-ADH、MDR002-PTGR、MDR003-FAS及MDR010-CAD等,不同种类间序列同源性在40%~90%之间.中链脱氢酶一般是以单聚体、二聚体或四聚体的形式存在.每个亚基含有两个结构部分[ The catalytic mechanism of Drosophila alcohol dehydrogenase: evidence for a proton relay modulated by the coupled ionization of the active site Lysine/Tyrosine pair and a NAD+ ribose OH switch 1 2010 ... 立体选择性羰基还原酶遵循顺序Bi-Bi 动力学催化机制催化手性醇的合成,酶与辅酶NAD(P)H结合组成全酶,底物进入酶的活性中心,形成酶-底物复合体,底物获得辅酶传递的质子被还原为手性醇,NAD(P)H失去质子被氧化为NAD(P)+,手性醇与NAD(P)+随后与酶分离,NAD(P)+可通过辅酶再生途径转化为NAD(P)H进入下一次催化反应[ Active site directed mutagenesis of 3β/17β-hydroxysteroid dehydrogenase establishes differential effects on short-chain dehydrogenase/reductase reactions 1 1997 ... 短链脱氢酶(SDRs)是一种非金属依赖酶,一般含有250~350个氨基酸残基.自19世纪70年代发现昆虫乙醇脱氢酶和细菌核糖醇脱氢酶以来,短链脱氢酶数量不断扩充,目前GenBank数据库中收录的短链脱氢酶的数量已超过99000种[ Origin and evolution of medium chain alcohol dehydrogenases 1 2013 ... 中链脱氢酶(MDRs)是一类约含350个氨基酸残基的锌或非锌-依赖型脱氢酶.根据迭代隐马尔可夫模型(HMMs),中链脱氢酶可分为86类,包括MDR001-ADH、MDR002-PTGR、MDR003-FAS及MDR010-CAD等,不同种类间序列同源性在40%~90%之间.中链脱氢酶一般是以单聚体、二聚体或四聚体的形式存在.每个亚基含有两个结构部分[ Conserved structural features and sequence patterns in the GroES fold family 1 1999 ... 中链脱氢酶(MDRs)是一类约含350个氨基酸残基的锌或非锌-依赖型脱氢酶.根据迭代隐马尔可夫模型(HMMs),中链脱氢酶可分为86类,包括MDR001-ADH、MDR002-PTGR、MDR003-FAS及MDR010-CAD等,不同种类间序列同源性在40%~90%之间.中链脱氢酶一般是以单聚体、二聚体或四聚体的形式存在.每个亚基含有两个结构部分[ Structure of the NADH-dependent thermostable alcohol dehydrogenase TADH from Thermus sp. ATN1 provides a platform for engineering specificity and improved compatibility with inorganic cofactor-regeneration catalysts 2 2014 ... 中链脱氢酶(MDRs)是一类约含350个氨基酸残基的锌或非锌-依赖型脱氢酶.根据迭代隐马尔可夫模型(HMMs),中链脱氢酶可分为86类,包括MDR001-ADH、MDR002-PTGR、MDR003-FAS及MDR010-CAD等,不同种类间序列同源性在40%~90%之间.中链脱氢酶一般是以单聚体、二聚体或四聚体的形式存在.每个亚基含有两个结构部分[
醛酮还原酶(AKRs)是一类含有320个左右氨基酸的非金属依赖型羰基还原酶,广泛存在于动物、植物、原核生物中,并大多以单体形式存在[ Structure of NADH‐dependent carbonyl reductase (CPCR2) from Candida parapsilosis provides insight into mutations that improve catalytic properties 3 2014 ... 中链脱氢酶(MDRs)是一类约含350个氨基酸残基的锌或非锌-依赖型脱氢酶.根据迭代隐马尔可夫模型(HMMs),中链脱氢酶可分为86类,包括MDR001-ADH、MDR002-PTGR、MDR003-FAS及MDR010-CAD等,不同种类间序列同源性在40%~90%之间.中链脱氢酶一般是以单聚体、二聚体或四聚体的形式存在.每个亚基含有两个结构部分[
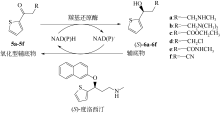
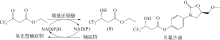
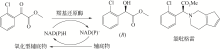
醛酮还原酶(AKRs)是一类含有320个左右氨基酸的非金属依赖型羰基还原酶,广泛存在于动物、植物、原核生物中,并大多以单体形式存在[ Subdivision of the MDR superfamily of medium chain dehydrogenases/reductases through iterative hidden Markov model refinement 1 2010 ... 中链脱氢酶(MDRs)是一类约含350个氨基酸残基的锌或非锌-依赖型脱氢酶.根据迭代隐马尔可夫模型(HMMs),中链脱氢酶可分为86类,包括MDR001-ADH、MDR002-PTGR、MDR003-FAS及MDR010-CAD等,不同种类间序列同源性在40%~90%之间.中链脱氢酶一般是以单聚体、二聚体或四聚体的形式存在.每个亚基含有两个结构部分[ Superfamilies SDR and MDR: from early ancestry to present forms. emergence of three lines, a Zn-metalloenzyme, and distinct variabilities 1 2010 ... 中链脱氢酶(MDRs)是一类约含350个氨基酸残基的锌或非锌-依赖型脱氢酶.根据迭代隐马尔可夫模型(HMMs),中链脱氢酶可分为86类,包括MDR001-ADH、MDR002-PTGR、MDR003-FAS及MDR010-CAD等,不同种类间序列同源性在40%~90%之间.中链脱氢酶一般是以单聚体、二聚体或四聚体的形式存在.每个亚基含有两个结构部分[ The aldo-keto reductase superfamily homepage 1 2003 ... 醛酮还原酶(AKRs)是一类含有320个左右氨基酸的非金属依赖型羰基还原酶,广泛存在于动物、植物、原核生物中,并大多以单体形式存在[ The diversity of microbial aldo/keto reductases from Escherichia coli K12 1 2013 ... 醛酮还原酶(AKRs)是一类含有320个左右氨基酸的非金属依赖型羰基还原酶,广泛存在于动物、植物、原核生物中,并大多以单体形式存在[ Comparative anatomy of the aldo-keto reductase superfamily 1 1997 ... 醛酮还原酶(AKRs)是一类含有320个左右氨基酸的非金属依赖型羰基还原酶,广泛存在于动物、植物、原核生物中,并大多以单体形式存在[ Aldo-keto reductase (AKR) superfamily: genomics and annotation 1 2009 ... 醛酮还原酶(AKRs)是一类含有320个左右氨基酸的非金属依赖型羰基还原酶,广泛存在于动物、植物、原核生物中,并大多以单体形式存在[ Human aldo-keto reductases: function, gene regulation, and single nucleotide polymorphisms 1 2007 ... 醛酮还原酶(AKRs)是一类含有320个左右氨基酸的非金属依赖型羰基还原酶,广泛存在于动物、植物、原核生物中,并大多以单体形式存在[ Biocatalytic properties of a recombinant aldo-keto reductase with broad substrate spectrum and excellent stereoselectivity 2011 Characterization and identification of three novel aldo-keto reductases from Lodderomyces elongisporus for reducing ethyl 4-chloroacetoacetate 2014 Genomic mining-based identification of novel stereospecific aldo-keto reductases toolbox from Candida parapsilosis for highly enantioselective reduction of carbonyl compounds 2014 Improved o-chlorobenzoylformate bioreduction by stabilizing aldo-keto reductase YtbE with additives 1 2014 ... (S)-氯吡格雷(Plavix)是一种选择性血小板凝集抑制剂,由法国赛诺菲(Snaofi)公司开发,用于治疗因血栓引起的心肌梗死和缺血性卒中,是目前世界上最畅销的药物之一.在已报道的(S)-氯吡格雷合成途径中,(R)-邻氯扁桃酸甲酯的合成是关键步骤( Microbial aldo-keto reductases 2 2002 ... 醛酮还原酶(AKRs)是一类含有320个左右氨基酸的非金属依赖型羰基还原酶,广泛存在于动物、植物、原核生物中,并大多以单体形式存在[
本文的其它图/表
|